El laboratorio biotecnológico argentino Inmunova anunció la publicación de los resultados del estudio clínico de Fase 2/3 del suero hiperinmune anti-SARS-CoV-2 en EClinicalMedicine, la prestigiosa revista médica con un riguroso sistema de revisión por pares y de acceso abierto publicada por The Lancet.
El equipo científico está compuesto por Gustavo Lopardo del Hospital Municipal Dr. Bernardo Houssay de la Provincia Buenos Aires; Waldo H. Belloso del Departamento de investigaciones del Hospital Italiano de Buenos Aires; Esteban Nannini, del Departamento de Enfermedades Infecciosas, del Sanatorio Británico, en la ciudad de Rosario; Mariana Colonna y Santiago Sanguinetti, ambos de Inmunova; y Vanesa Zyberman del Consejo Nacional de Investigaciones Científicas y Técnicas de Argentina, entre otros.
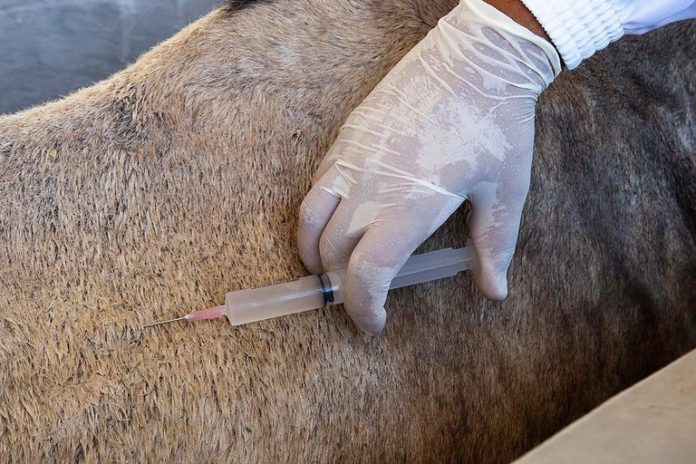
En el texto se da a conocer que el suero hiperinmune anti-SARS-CoV-2 (CoviFab®) es un medicamento biológico para tratar la enfermedad COVID-19 moderada a severa, cuyo desarrollo llevó adelante Inmunova a partir de su experiencia en ingeniería de proteínas. Es una inmunoterapia de anticuerpos policlonales equinos con capacidad neutralizante contra el nuevo coronavirus basada en inmunización pasiva. Esto significa que al paciente se le administran anticuerpos contra el agente infeccioso para bloquearlo y evitar que se propague en el organismo.
El hallazgo argentino tiene carácter oportuno y antiocipatorio, ya que antes de que se cumpliera un año de la aparición del coronavirus SARS-CoV-2, que originó la pandemia de COVID-19 por la que ya se infectaron 135 millones de personas y murieron más de 2,9 millones en todo el mundo (según datos del Johns Hopkins University & Medicine Resource Center), la Argentina ya tenía desarrollado y aprobado por la ANMAT un tratamiento para pacientes con enfermedad moderada o grave altamente efectivo.
La terapia con este suero equino demostró un adecuado perfil de seguridad en la población evaluada; los eventos adversos de especial interés fueron leves y no requirieron la interrupción de la infusión ni impidieron la administración de la segunda dosis.
En cuanto a eficacia, demostró mejoría estadísticamente significativa en al menos 2 categorías de la escala ordinal de evaluación clínica de 8 puntos de la OMS a los 14 y 21 días; diferencia estadísticamente significativa en el tiempo de mejora en al menos 2 categorías ordinales de la OMS o alta hospitalaria en el grupo tratado con el suero hiperinmune frente al placebo (14,2 versus 16,3 días, respectivamente) y cambios favorables en la escala ordinal de la OMS durante los 28 días de seguimiento. Esta escala establece categorías como la externación sin o con limitación en las actividades, hospitalización sin o con necesidad de oxígeno, soporte de asistencia respiratoria mecánica, entre otras.
Mostró una tendencia favorable, aunque no significativa estadísticamente, al beneficio clínico en los parámetros más importantes para medir la progresión de los pacientes: reducción en la mortalidad de 44% en los pacientes con COVID-19 severa, de la internación en terapia intensiva en 29% y el requerimiento de asistencia respiratoria mecánica en 33%, frente al placebo.
Los resultados del estudio clínico de Fase 2/3 del suero hiperinmune anti-SARS-CoV-2 habían sido presentados a la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT), que el 22 de diciembre 2020 autorizó el medicamento mediante un Registro Bajo Condiciones Especiales –modalidad establecida en la Disposición 4622/2012 de esta autoridad reguladora–.
La autorización, que se fundamenta en el cociente favorable beneficio/riesgo en función de la evidencia científica demostrada, aprobó su uso en situación de pandemia para el tratamiento de pacientes adultos con enfermedad COVID-19 moderada a severa, dentro de 10 días del inicio de los síntomas, con consentimiento informado y monitoreo de seguridad y eficacia para continuar recopilando datos durante un año. Enfermedad moderada a severa según los criterios 3, 4 y 5 de la escala ordinal de evaluación clínica de 8 puntos de la OMS: paciente hospitalizado sin necesidad de oxígeno, uso de oxígeno con máscara y ventilación no invasiva u oxígeno de alto flujo.

La ventaja que le ven los desarrolladores del suero equino hiperinmune es la escalabilidad relativamente rápida, ya que uno puede inmunizar 10 caballos, vacunándolos con una partícula, un antígeno técnicamente del virus; se pueden hacer 10, 100 o 200 sueros si hace falta para abastecer a toda la demanda.
Suero hiperinmune anti-SARS-CoV-2 desde adentro
La ventaja de los anticuerpos policlonales es que reconocen y unen en varias regiones a la molécula clave del virus (el dominio RBD de la proteína Spike), bloqueando los sitios de interacción con su receptor humano. Como ventaja adicional, pueden producirse rápidamente a gran escala.
Este tratamiento es fruto del trabajo llevado adelante por Inmunova junto con el Instituto Biológico Argentino (BIOL), mAbxience, Grupo Insud, con la participación de instituciones públicas y privadas, así como el apoyo de la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación dependiente del Ministerio de Ciencia, Tecnología e Innovación y del Fondo Nacional de Desarrollo Productivo (FONDEP) dependiente del Ministerio de Desarrollo Productivo.
Según lo publicado en EClinical Medicine de The Lancet, sobre este hallazgo del suero hiperinmune: “Este estudio tuvo varias limitaciones. Dado que el efecto de INM005 fue más notable en aquellos con enfermedad grave, el bajo número de pacientes incluidos en esta categoría y la variabilidad observada en el día 28 nos impidió alcanzar el criterio de valoración principal con significación estadística. Otra limitación del estudio es que la edad general de la población era más joven que la de otras series de estudios similares, lo que hace que este hallazgo sea menos generalizable. Este ensayo clínico evaluó los EpAbs en pacientes con COVID-19 de moderado a grave. INM005 podría probarse en otras etapas clínicas, incluidas las enfermedades tempranas y críticas. Otra limitación incluye el momento de la primera medición de carga viral tras el inicio del tratamiento, ya que se realizó cuando la mayoría de los pacientes habrían alcanzado niveles bajos de forma espontánea, lo que nos impide realizar un análisis adecuado de INM005 en este parámetro”.
“En el grupo de pacientes con enfermedad grave, encontramos un efecto a favor de INM005 en el punto final primario en los días 14 y 21. En consecuencia, en este subgrupo, observamos una disminución del 45% en la mortalidad entre los que recibieron INM005, aunque el efecto no fue estadísticamente significativo. Los resultados en la población severa no alcanzaron la significación estadística probablemente debido al tamaño reducido de la muestra en este subgrupo. Este estudio agregó evidencia inicial para el uso de inmunoterapia pasiva en pacientes con enfermedad grave por COVID-19”.
PARA LEER EL ESTUDIO HACER CLICK EN EL SIGUIENTE LINK:

Somos un periódico de entretenimiento, música, películas y algo más









